吴彤/李智慧主任及陶勇教授合作团队:首次报道CAR-T桥接移植后Purtscher样视网膜病变病例
2026-2-13随着CAR-T细胞治疗在复发/难治血液肿瘤中的广泛应用,越来越多患者获得深度缓解,并成功进入造血干细胞移植阶段。与此同时,多线免疫治疗的叠加应用,也使移植后并发症的表现更加复杂。如何在这一背景下,及早识别非典型并发症、避免延误干预,成为当前临床实践中亟需关注的重要课题。
近日,高博医疗集团吴彤主任与首都医科大学附属北京朝阳医院陶勇教授为共同通讯作者,高博医疗集团李智慧主任为第一作者的合作团队,在Frontiers in Immunology发表病例研究,在全球首次系统报道了一例CAR-T桥接异基因造血干细胞移植后发生Purtscher样视网膜病变(PLR)的罕见病例,并深入探讨其与移植相关血栓性微血管病(TA-TMA)之间的潜在机制关联。
李智慧主任介绍,在临床实践中,一些并发症并不以典型血液学异常起病,而可能首先表现为局部、非特异性的症状,增加了早期识别的难度。基于这一背景,团队对本例在CAR-T联合移植后出现的罕见眼部病变进行了系统梳理与分析,希望提示临床在复杂免疫治疗背景下,更加关注非典型表现背后的系统性意义。

病例概述
从多线免疫治疗到移植:复杂治疗路径的回顾
本研究报道一例复发急性B淋巴细胞白血病(B-ALL)患儿。患儿初诊后接受规范治疗获得缓解,约2.5年后出现首次血液学复发。为控制病情,患儿接受CD19 CAR-T细胞治疗并获得缓解,随后为进一步巩固疾病控制并降低抗原逃逸风险,序贯接受CD22 CAR-T细胞治疗。
2024年,患儿病程再次进展并出现复发(伴髓外浸润)。在该阶段,治疗策略转向抗体类免疫治疗以争取再缓解:患儿接受抗CD22抗体药物偶联物(奥加伊妥珠单抗),并联合免疫调节治疗(如贝利尤单抗)等,最终在获得移植窗口后行异基因造血干细胞移植(allo-HSCT)。
突发视力变化的识别与处理:PLR的影像学特征与治疗反应
移植后约160天,患儿出现突发无痛性视力下降伴视物变形,无外伤史。经眼底照相(图1A&B)、光学相干断层扫描(OCT,图2A&B)及荧光素眼底血管造影等系统眼科评估后,确诊为Purtscher样视网膜病变(PLR)。
患儿首先接受雷珠单抗左眼玻璃体腔内注射治疗(0.5 mg),每月一次。首次注射后第6天,左眼视力较前明显改善,同时视盘水肿及视网膜出血明显减轻(图1D、图2D)。
为进一步评估病变机制,研究团队对房水进行流式微球阵列(CBA)检测,发现碱性成纤维细胞生长因子(bFGF)与血管细胞黏附分子-1(VCAM-1)水平显著升高,提示血-视网膜屏障受损。
在此期间,患儿右眼视力迅速下降,伴随视网膜出血、棉絮斑增多及视神经盘水肿加重(图1C、图2F)。随后,研究团队对右眼启动雷珠单抗玻璃体腔注射(0.5 mg)。
右眼首次注射后第8天,左眼视力继续改善;虽然右眼视力未进一步提升,但双眼眼底检查均显示视网膜出血、棉絮斑及视神经盘水肿明显减轻(图1E、F;图2E、F),提示抗VEGF治疗在控制眼底微血管病变方面具有积极作用。
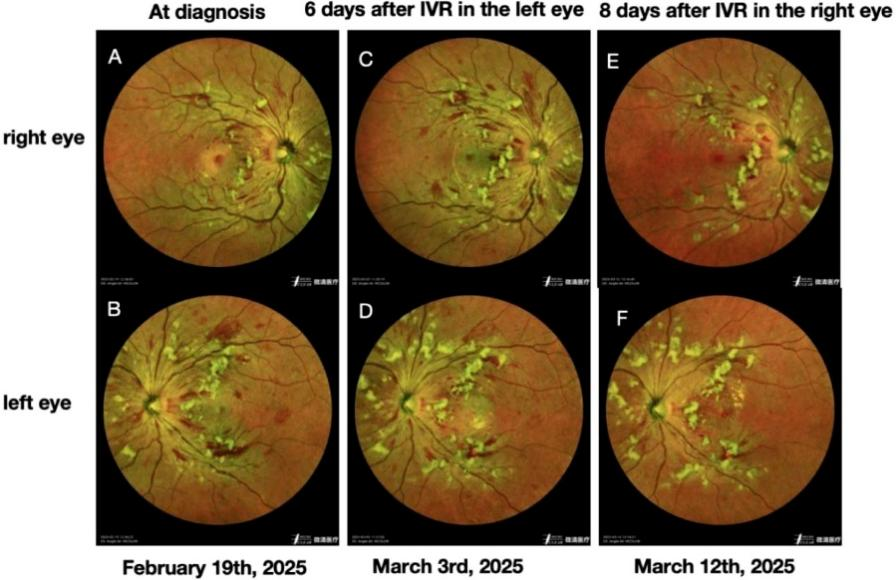
图1:患儿双眼眼底照相
(A,B)双眼后极部可见多发视网膜出血、棉絮斑及黄白色Purtscher斑(Purtscher flecken),其中左眼受累更为广泛
(C)与前期观察相比,右眼视网膜出血、棉絮斑及Purtscher斑明显增多。
(D)左眼行雷珠单抗玻璃体腔内注射后第6天,视网膜出血较前部分吸收,棉絮斑及Purtscher变化不明显。
(E)右眼行雷珠单抗玻璃体腔内注射后第8天,视网膜出血、棉絮斑及Purtscher斑较前明显减轻。
(F)左眼行雷珠单抗玻璃体腔内注射后第15天,可见视网膜出血进一步吸收,棉絮斑及Purtscher斑亦较前减少。
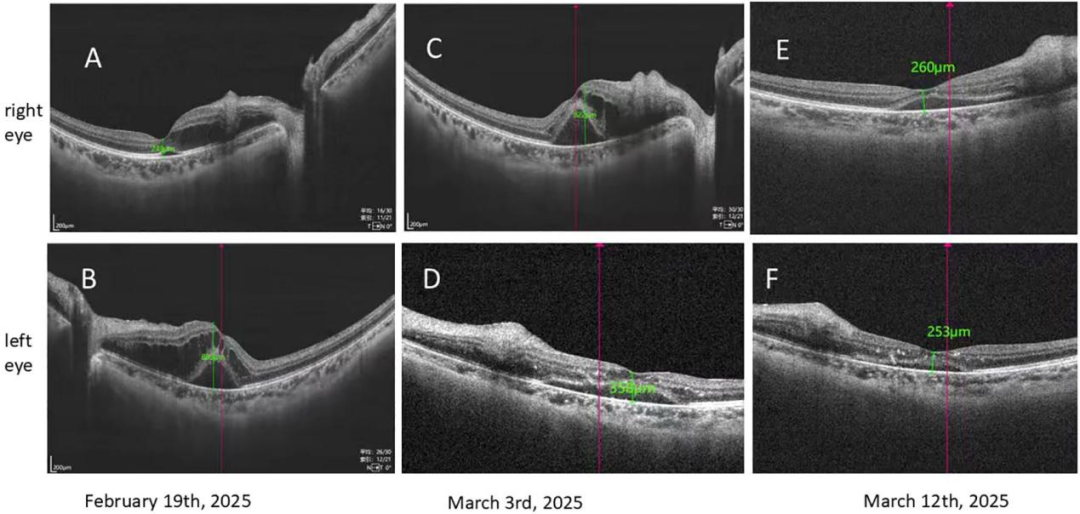
图2:患儿双眼OCT图像
(A)右眼(2月19日):视网膜内层水肿及增厚,可见囊样黄斑水肿,厚度约249μm。
(B)左眼(2月19日):视网膜内层水肿及明显增厚,囊样黄斑水肿厚度约885μm,并可见多个局灶性高反射灶。
(C)右眼(3月3日):视网膜内层水肿及增厚进一步加重,囊样黄斑水肿厚度约822μm,较前明显增加。
(D)左眼(3月3日):视网膜内层水肿及增厚减轻,囊样黄斑水肿厚度约358μm,较前明显下降。
(E)右眼(3月12日):视网膜内层水肿及增厚明显改善,囊样黄斑水肿厚度约253μm,较既往检查显著减轻。
(F)左眼(3月12日):囊样黄斑水肿厚度约260μm,与前次影像相比变化不大。
从眼底病变到系统评估:
TA-TMA的识别与管理
在眼部病变评估与治疗过程中,研究团队同步对患儿进行系统性检查。移植后第179天,淋巴细胞亚群分析显示CD4/CD8比值为0.22,B细胞比例5.05%,NK细胞比例21.68%,提示免疫重建受限。
至移植后第194天,患儿出现重度血小板减少(最低40×109/L)、大量蛋白尿(24h尿蛋白2400mg)、肾功能损害(血肌酐133.9μmol/L)及补体激活(C5b-9 298ng/mL),并伴多腔隙浆膜腔积液。
经系统评估,排除了移植物抗宿主病(GVHD)及钙调神经磷酸酶抑制剂毒性等因素,结合外周血破碎红细胞增多(0.8%),最终明确诊断为移植相关血栓性微血管病(TA-TMA)。
针对TA-TMA,患儿接受去纤苷和依库珠单抗治疗,并配合利尿、降压及毛细血管渗漏对症支持治疗后,整体病情趋于稳定。
总结及展望
李智慧主任指出,本研究首次系统报道了复发B-ALL患儿在CAR-T桥接异基因造血干细胞移植后发生Purtscher样视网膜病变的病例;同时,在本病例中眼底表现的出现早于部分系统性改变,为理解移植后微血管相关并发症的发生过程提供了新的观察视角。在免疫治疗与移植不断融合的背景下,临床需要更加重视突发视力变化等非典型症状,通过影像学评估与系统性检查相结合,及早识别潜在的微血管病变或补体相关异常并启动相应管理。通过多学科协作与精细化评估,有助于进一步优化移植后并发症的识别与处理路径,提升整体治疗安全性与预后。










